Crée en 2008, l’équipe 2 intitulée « Thérapies innovantes dans les leucémies myéloïdes et les cellules souches hématopoïétiques » décrypte les mécanismes moléculaires et cellulaires impliqués dans la différenciation physiologique et pathologique des cellules souches hématopoïétiques avec un intérêt cardinal pour les cellules du lignage myéloïde. Nous souhaitons ainsi proposer de nouvelles opportunités thérapeutiques pour des hémopathies myéloïdes incurables les SMD, les LAMs et la LMMC. Les progrès récents de la diversité génétique des SMD, des LAM et de la LMMC ont conduit au développement de thérapies plus efficaces, mais leur intégration à une approche clinique standardisée fait encore débat. Afin de contribuer au développement et à la validation de thérapies innovantes pour ces hémopathies, nous devons mieux comprendre les mécanismes moléculaires impliqués dans la transformation des cellules myéloïdes. Dans ce contexte, notre équipe étudie la régulation de l’apoptose, de l’autophagie, de la ferroptose, du stress oxydatif, de la différenciation et de la reprogrammation des cellules myéloïdes. Nos projets s’inscrivent dans une recherche fondamentale et appliquée, avec l’objectif de transférer nos découvertes du laboratoire vers la clinique à travers la mise au point de thérapies innovantes au bénéfice des patients.

Projets

G. RobertChargé de recherche
Mail guillaume.robert@univ-cotedazur.fr

P. AubergerDirecteur de recherche
Mail patrick.auberger@univ-cotedazur.fr

Le lysosome est un organelle clé pour la prise en charge et la dégradation des protéines à travers un spectre de processus tel que la Macroautophagie et l’Autophagie médiée par les chaperonnes (CMA).
Dans le cadre de nos recherches nous avons mis en évidence l’importance de cet organelle au cours du vieillissement et son importance dans la genèse des leucémies myéloïdes. Nous étudions actuellement à travers des modèles murins originaux l’impact de l’invalidation d'une protéine lysosomale sur la dérégulation du compartiment hématopoïétique et la genèse des leucémies myéloïdes.
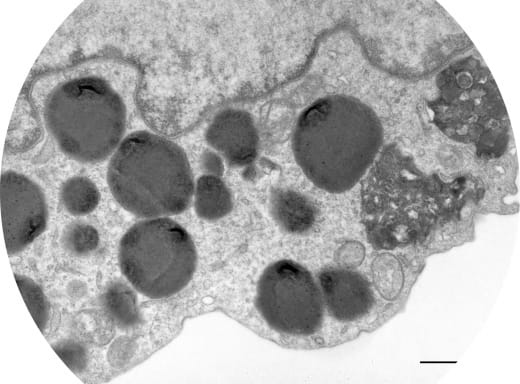
Nous développons en collaboration avec l’Institut de Chimie de Nice des molécules chimériques dites « biodégradeurs » capables de cibler des protéines oncogéniques impliquées dans le leucémies et de les adresser au sein du lysosome.

C. FavreauIngénieur(e) d’études
Mail cecile.favreau@univ-cotedazur.fr

a. RivaultDoctorant(e)
Mail adele.rivault@etu.univ-cotedazur.fr

C. SavyIngénieur(e) d’études
Mail coline.savy@univ-cotedazur.fr

M. BourgoinIngénieur(e) d’études
Mail maxence.bourgoin@univ-cotedazur.fr

A. JacquelDirecteur de recherche
Mail arnaud.jacquel@univ-cotedazur.fr

P. AubergerDirecteur de recherche
Mail patrick.auberger@univ-cotedazur.fr
Mon groupe se concentre sur l'étude des cellules immunosuppressives myéloïdes, comme les macrophages anti-inflammatoires (macrophages associés aux leucémies et TAMs) et les MDSCs (Myeloid-derived suppressor cells), dans les leucémies myéloïdes (Leucémie Aigüe Myéloïde, Syndrome MyéloDysplasique et Leucémie MyéloMonocytaire Chronique). La principale fonction de ces cellules dans le cancer est d'inhiber la réponse immunitaire antitumorale. Par conséquent, la compréhension des mécanismes moléculaires impliqués dans la génération des macrophages anti-inflammatoires et des MDSCs pourrait permettre de développer de nouvelles stratégies thérapeutiques. Une meilleure caractérisation de leur origine, de leur phénotype et de leur capacité à déclencher une réponse antitumorale, ainsi que de la manière dont ces différentes sous-populations immunosuppressives myéloïdes pourraient être affectées par des thérapies anticancéreuses, est indispensable pour pouvoir les cibler/reprogrammer sélectivement dans les différents types de leucémies.

E. KerreneurDoctorant(e)
Mail emeline.kerreneur@etu.univ-cotedazur.fr

M. BourgoinIngénieur(e) d’études
Mail maxence.bourgoin@univ-cotedazur.fr

C. DelabyDoctorant(e)
Mail chloe.delaby@etu.univ-cotedazur.fr

M. FajollesIngénieur(e) d’études
Mail morgane.fajolles8@etu.unice.fr

A. AouadIngénieur(e) d’études
Mail amaury.aouad@univ-cotedazur.fr
Publications
Focus
Dual Covalent Inhibition of PKM and IMPDH Targets Metabolism in Cutaneous Metastatic Melanoma.Auteurs Zerhouni M, Martin AR, Furstoss N, Gutierrez VS, Jaune E, Tekaya N, Beranger GE, Abbe P, Regazzetti C, Amdouni H, Driowya M, Dubreuil P, Luciano F, Jacquel A, Tulic MK, Cluzeau T, O'Hara BP, Ben-Sahra I, Passeron T, Benhida R, Robert G, Auberger P, Rocchi S
Cancer research Juin 2021
IL-34 and CSF-1 display an equivalent macrophage differentiation ability but a different polarization potential.Auteurs Boulakirba S, Pfeifer A, Mhaidly R, Obba S, Goulard M, Schmitt T, Chaintreuil P, Calleja A, Furstoss N, Orange F, Lacas-Gervais S, Boyer L, Marchetti S, Verhoeyen E, Luciano F, Robert G, Auberger P, Jacquel A
Scientific reports Jan 2018
D'autres publications récentes
Emerging role of glutathione peroxidase 4 in myeloid cell lineage development and acute myeloid leukemia.Auteurs Auberger P, Favreau C, Savy C, Jacquel A, Robert G
Cellular & molecular biology letters Jul 2024
HSPA8 chaperone complex drives chaperone-mediated autophagy regulation in acute promyelocytic leukemia cell differentiation.Auteurs Rafiq S, Mungure I, Banz Y, Niklaus NJ, Kaufmann T, Müller S, Jacquel A, Robert G, Auberger P, Torbett BE, Muller S, Tschan MP, Humbert M
Pharmacology Apr 2024
Improving nutritional status after allogeneic stem cell transplantation: results of phase 2 ALLONUT clinical trial.Auteurs Estran S, Loschi M, Benachour S, Soldati A, Chiche E, Sammut R, Robert G, Jacquel A, Chibois J, Schneider S, Cluzeau T
Bone marrow transplantation Mar 2024
Voir toutes les publicationsBrevets
Co-inventeurs A. Jacquel, P. Auberger, M. Loschi, G. Robert, M. Bourgoin, M. Fajolles
Co-inventeurs O. Dufies, P. Chaintreuil, J. Courjon, A. Jacquel, P. Auberger, L. Boyer
Co-inventeurs A. Jacquel, P. Chaintreuil, G. Robert, P. Auberger
Rencontre avec les cliniciens
Le Vendredi 26 Novembre 2021, notre équipe a rencontré le service d'hématologie clinique de l'hopital l'archet du Pr. Thomas Cluzeau pour faire un bilan des projets 2021 et définir les collaborations à venir pour 2022 ....
Rencontre avec les donateurs
Le Mercredi 8 Décembre 2021, notre équipe a rencontré la famille Duplan et les membres du comité départemental 06 de la Ligue nationale contre le cancer . Cette journée d'échange nous a permis de présenter nos thèmatiques de recherche à cette famille touché de prés par la leucémie. La seconde partie de cette rencontre fut consacrée à un échange entre la famille, les membres du comité qui ont pu poser aux chercheurs toutes leurs questions sur les leucémies et les traitements en cours de developpement clinique. Cet échange s'est conclu par la remise d'un chèque important de soutien à nos recherches.












